成品小鼠皮肤疾病模型
- 基本信息
- 数据验证
- FAQ
品系描述
人乳头瘤病毒(HPV)属于双链 DNA 肿瘤病毒家族,其感染具有高度组织特异性,主要侵袭人体皮肤与粘膜上皮组织,是引发尖锐湿疣等常见性传播疾病的病原体。流行病学研究显示,高危型 HPV 持续感染是宫颈癌发生发展的必要条件,其中HPV16型在全球宫颈癌组织中的检出率高达 50%,被证实为驱动宫颈上皮细胞恶性转化的关键致癌亚型。
明迅生物研发的HPV-16宫颈癌小鼠,通过先进的基因编辑技术,构建了HPV16致癌基因的可控表达模型。该模型将HPV16的 E6/E7基因定点整合至小鼠Rosa26安全位点,并搭载Krt14启动子驱动的CreERT2重组酶系统。在未注射Tamoxifen(他莫昔芬)时, HPV16 E6/E7基因处于转录沉默状态;当给予Tamoxifen激活creERT2后,可实现K14阳性上皮组织(如宫颈、皮肤等)中HPV16 E6/E7基因的特异性、高强度表达,注射后约4周稳定出现相关病理表型。
-
数据验证Rosa26tm1(CAG-LSL-HPV16 E6E7)/MCL纯合与杂合小鼠的表型对比Rosa26tm1(CAG-LSL-HPV16 E6E7)/MCL;Krt14tm1(creERT2)/MCL 杂合与纯合小鼠皮肤病理表型对比。在他莫昔芬诱导 HPV16 E6/E7基因表达后,HPV16 E6E7杂合的小鼠呈现典型的皮肤病变特征,包括表皮层增生、组织厚度显著增加,同时伴随细胞核体积增大、异染色质减少等细胞学异常改变。与纯合子小鼠相比,杂合小鼠虽然展现出相似的病理趋势,但病变累及范围、细胞形态学改变程度及组织学异常的整体严重程度均较低。本结果通过HE染色对皮肤组织切片进行形态学分析,比较不同基因型小鼠的病理差异,证明HPV16 E6/E7基因剂量与病变进展有关联。
图 5:Rosa26tm1(CAG-LSL-HPV16 E6E7)/MCL;Krt14tm1(creERT2)/MCL杂合与纯合小鼠皮肤病理表型对比。与纯合子小鼠相比,杂合小鼠虽然展现出相似的病理趋势,但病变累及范围、细胞形态学改变程度及组织学异常的整体严重程度均较低。
-
数据验证图3: Rosa26tm1(CAG-LSL-HPV16 E6E7)/MCL纯合小鼠耳部皮肤:在他莫昔芬诱导HPV16E6/E7基因表达后,HPV16 E6E7杂合的小鼠呈现典型的皮肤病变特征,包括表皮层增生、组织厚度显著增加,同时伴随细胞核体积增大、异染色质减少等细胞学异常改变。
-
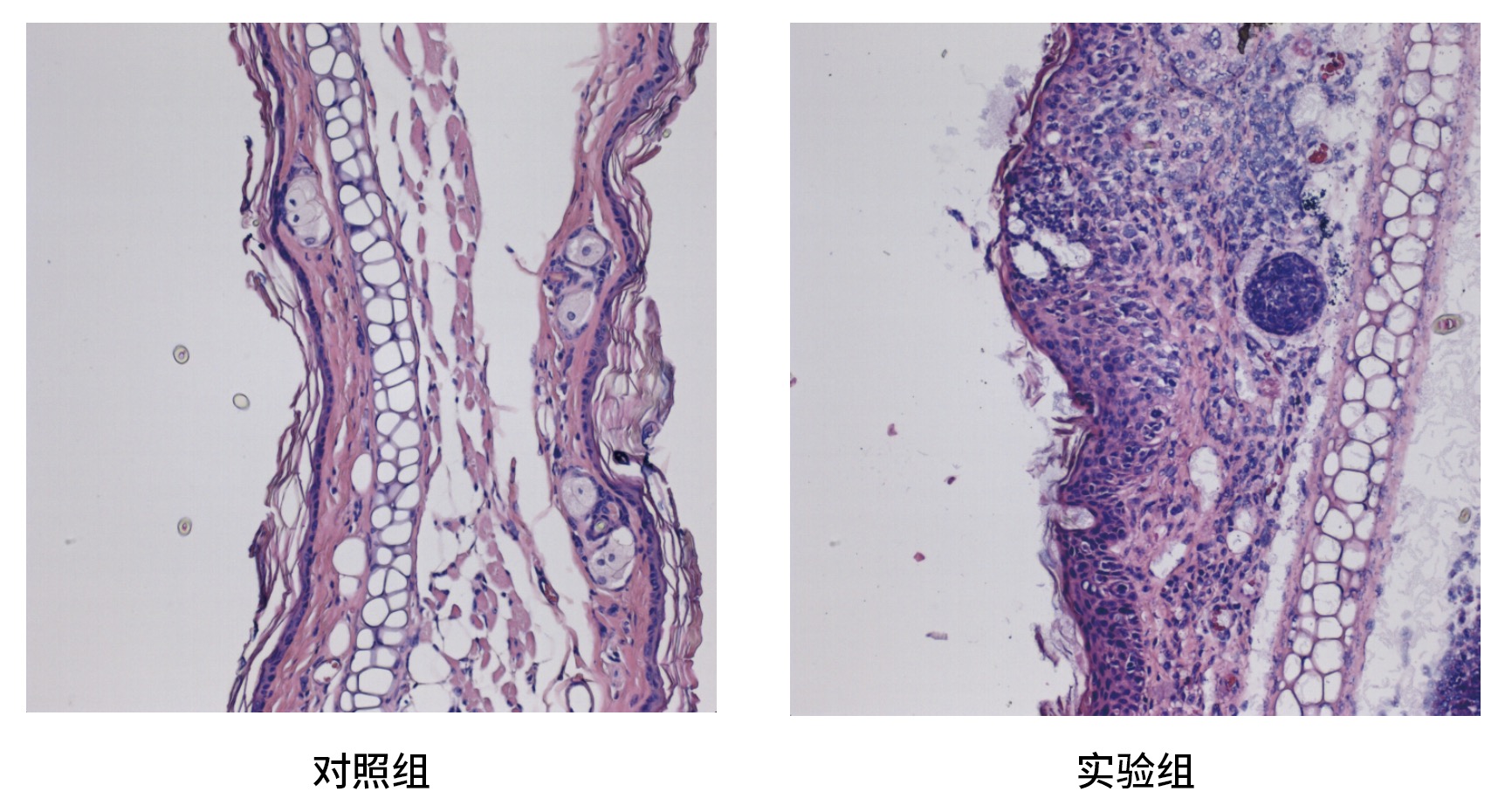
数据验证组织病理验证Tamoxifen注射完成后第五周小鼠组织病理特征。经 H&E 染色及组织学分析显示,与对照组相比,实验组小鼠皮肤组织呈现显著病理改变:+tamoxifen的实验组相对对照组,皮肤增生厚度增加、细胞核变大、核质比失调,同时异染色质密度降低,呈现低分化肿瘤细胞特征。上述结果证实他莫昔芬诱导的HPV16 E6/E7基因表达可直接驱动皮肤上皮细胞发生增生性病变及恶性转化倾向。
图2: Rosa26tm1(CAG-LSL-HPV16 E6E7)/MCL纯合小鼠面部皮肤:在他莫昔芬诱导HPV16 E6/E7基因表达后,HPV16 E6E7杂合的小鼠呈现典型的皮肤病变特征,包括表皮层增生、组织厚度显著增加,同时伴随细胞核体积增大、异染色质减少等细胞学异常改变。
-
数据验证HPV16-E6/E7诱导前后的表达水平CreERT2重组酶由 K14 启动子驱动,在特定上皮组织中呈持续性表达状态,但仅在Tamoxifen激活后获得Cre重组酶活性。给药前,CreERT2处于失活状态,Rosa26位点中位于LoxP序列之间的终止元件(LSL)阻断HPV16 E6/E7及荧光素酶(Luci)基因转录;注射Tamoxifen(10mg/ml,100μl/只/天,连续3天)后,激活的CreERT2特异性切除LoxP间终止序列,触发E6/E7及Luci基因的条件性表达。本实验通过 RT-qPCR 技术,在给药后第3天从RNA 水平验证了CreERT2系统的激活效率及HPV16 E6/E7基因的诱导表达效果,结果与预期设计一致。
图2:他莫昔芬(Tamoxifen)诱导CreERT2系统激活及HPV16 E6/E7基因条件性表达验证。E6、E7、Lucifer-ase在添加tamoxifen的实验组中高表达,而在不加tamoxifen的对照组中不表达;实验组(+tamoxifen,n=6只),对照组(-tamoxifen,n=5只),WT组(n=3只)。
-
数据验证小鼠外观病变特征a.实验组设置:选取6周龄以上的FVBn-LSL-HPV16 E6E7/Krt14-creERT2转基因小鼠,腹腔注射浓度为10mg/ml的他莫昔芬Tamoxifen)溶液,按100μl/只/天的剂量连续给药5天,通过激活CreERT2重组酶系统,诱导HPV16 E6/E7基因在K14阳性上皮组织中特异性表达。
b.对照组设置:同周龄同品系转基因小鼠作为对照,以等体积蒸馏水进行腹腔注射,操作流程与实验组保持一致,排除注射操作本身对实验结果的干扰。
c.观察与记录:给药结束后,两组小鼠均在标准SPF级环境中继续饲养,每日进行健康状态监测,并每周定时拍摄小鼠外观照片。结果显示,实验组小鼠在注射他莫昔芬后第2周,开始出现面部皮肤增厚、褶皱增多等增生性病变,且随着时间推移,病变范围逐渐扩展,角质层异常堆积、局部组织隆起;而对照组小鼠全程未出现任何皮肤形态学改变。图示为给药后第5周两组小鼠的外观对比。
图 1:他莫昔芬(Tamoxifen)诱导HPV16 E6/E7基因表达 5 周后小鼠上皮组织表型变化。实验组小鼠面部皮肤显著增厚、褶皱堆积,脚趾部位出现角质层异常增生及组织隆起,并伴随局部毛发脱落;而对照组同品系小鼠无病理改变。
-
q如何进行种群管理a普通 KI 小鼠是将外源基因插入基因组的任意位点,可能是随机整合,也可能依赖简单同源重组定位。

 会员中心
会员中心 EN
EN
 姓名*
姓名*
 电话*
电话*
 邮箱*
邮箱*
 公司*
公司*
 信息*
信息*

